| Главная » Файлы » Химия » Задачи и примеры по химии |
2NO(г) + O2(г) = 2NO2(г)
| 04.11.2013, 00:17 | |
| Как изменится скорость реакции: 2NO(г) + O2(г) = 2NO2(г); если уменьшить объем реакционной смеси в 3 раза? Решение : До изменения объема скорость реакции выражалась уравнением: v = k[NO]²[O2]. Вследствие уменьшения объема концентрация каждого из реагирующих веществ возрастет в три раза. Следовательно: ν = k(3[NO])²(3[О2]) = 27k[NO]²[О2]. Сравнивая выражения для ν и ν`, находим, что скорость реакции возрастает в 27 раз. Зависимость скорости реакции (или константы скорости реакции) от температуры может быть выражена уравнением: 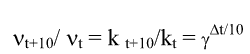 Здесь vt и kt - скорость и константа скорости реакции при температуре t °C; νt+10 и kt+10 - те же величины при температуре (t + 10) °C; γ - температурный коэффициент скорости реакции, значение которого для большинства реакций равно 2 - 4 (правило Вант-Гоффа). В общем случае, если температура изменилась на t °C, последнее уравнение преобразуется к виду: или 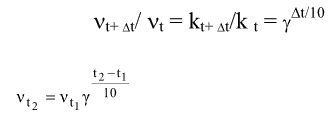 (4.2.3) (4.2.3)
| |
| Просмотров: 1518 | Загрузок: 0 | | |
| Всего комментариев: 0 | |
Категории раздела
| Нестандартные задачи по химии [57] |
| Задачи и примеры по химии [341] |
| Растворы,смеси, сплавы [137] |
| Формулы ,Таблицы, Правила [32] |
| Тесты [114] |
| Аналитическая химия [15] |
| Физическая Химия [113] |
| Расчетные задачи и примеры [165] |
| Задачи-головоломки [107] |
| Химические уравнения [118] |
| Лабораторные работы [10] |
| Коллоидная химия [17] |
| Электрохимия [31] |
Друзья сайта