| Главная » Статьи » Химия » Химия |
Графический метод решения химических задачВВЕДЕНИЕ Решение расчетных задач – важнейшая составная часть школьного предмета «химия», так как это знаний. Чтобы научиться химии, систематическое изучение известных истин химической науки должно сочетаться с смостоятельным поиском решения сначала малых, а затем и больших проблем. 1. Математические способы решения расчетных задач по химии Как бы ни были интересны теоретические разделы учебника и качественные опыты практикума, они недостаточны без численного подтверждения выводов теории и результатов эксперимента: ведь химия – количественная наука. Включение задач в учебный процесс позволяет реализовать следующие дидактические принципы обучения: 2) достижение прочности знаний и умений; 4) реализация предпрофильного и профильного политехнического обучения. Решение задач является одним из звеньев в прочном усвоении учебного материала, так как формирование В решении химических задач целесообразно использовать алгебраические приёмы. В этом случае исследование и анализ ряда задач сводятся к преобразованиям формул и подставлению известных величин в конечную формулу или алгебраическое уравнение. Задачи по химии похожи на задачи по математике, и некоторые количественные задачи по химии (особенно на «смеси») удобнее решать через систему уравнений с двумя неизвестными. Рассмотрим несколько таких задач Задача 1. Смесь карбонатов калия и натрия массой 7 г обработали серной кислотой, взятой в избытке. Решение . Составляем уравнений реакций:
Над уравнениями реакций записываем введенные обозначения, под уравнениями реакций записываем данные, полученные по уравнениям реакций, и составляем систему уравнений с двумя неизвестными: х/106 = у/22,4 (1) (7-х)/138=(1,344-у) (2) Из первого уравнения выражаем у через х: у = 22,4х/106 (3) (1,344-22,4х/106)•138=22,4•(7-х). Решаем уравнение (4) относительно х. 185,472-29,16х=156,8-22,4х 6,76х=28,672 х=4,24 Следовательно, масса карбоната натрия равна 4,24 г. Массу карбоната калия находим вычитанием из общей массы смеси карбонатов массы карбоната 7г-4,24г=2,76г. Массовые доли карбонатов находим по формуле: w=(mком-та/mобщая)•100% w(Na2CO3)=(4.24/7)•100%=60.57% w(K2CO3)=(2.76/7)•100%=39.43%. Ответ: массовая доля карбоната натрия равна 60,57%, массовая доля карбоната калия равна 39,43%. Задача 2. Смесь карбонатов калия и натрия массой 10 г растворили в воде и добавили избыток соляной кислоты. Выделившийся газ пропустили через трубку с пероксидом натрия. Образовавшегося кислорода Решение. Составляем уравнения реакций:
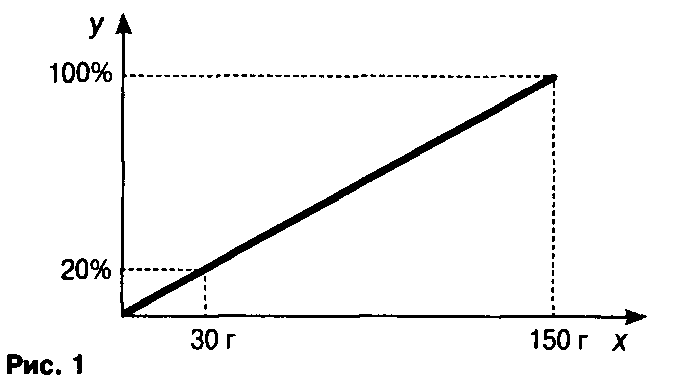
По уравнению (4) рассчитаем объем кислорода, образовавшегося в процессе реакции (3). Для этого через х в уравнении обозначим объём кислорода и, исходя из объёма водорода, составим пропорцию и решим её относительно х: 1,9/44,8=х/22,4; х=1,9•22,4/44,8; х=0,95л (объём выделившегося кислорода). Исходя из уравнения (3), рассчитаем объём углекислого газа, образовавшегося при обработке смеси карбонатов натрия и калия избытком соляной кислоты. Для этого составим пропорцию: х/44,8=0,95/22,4; х=0,95•44,8/22,4; х=1,9л. Через у л обозначим объём газа, выделившегося в процессе реакции (1), а через (1,9-у)л – объём х/106=у/22,4 (5) (10-х)/138=(1,9-у)/22,4 (6) Из уравнения (5) выражаем у через х и подставляем в уравнение (6): у=22,4х/106 (10-х)/138=(1,9-22,4х/106)/22,44 (7). Уравнение (7) решаем относительно х: (1,9-22,4х/106)•138=22,4•(10-х); 262,2-29,16х=224-22,4х; 6,76х=38,2; х=5,65г (масса карбоната натрия). Масса карбоната калия находится как разность между массой смеси карбонатов натрия и калия 10-5,65=4,35г (масса карбоната калия). w(Na2CO3)=(5,65/10)•100% w(Na2CO3)=56.5% w(K2CO3)=(4.35/10)•100% w(K2CO3)=43.5%/ Ответ: массовая доля карбоната натрия равна 56,5%, массовая доля карбоната калия равна 43,5%. Задачи для самостоятельного решения Задача 3 Смесь железа и цинка массой 12,1 г обработали избытком раствора серной кислоты. температура – 364К). Найдите массовую долю железа в смеси. Задача 4 Смесь метиловых эфиров уксусной кислоты и пропионовой кислоты массой 47,2г обработали 83,4мл раствора гидроксида натрия с массовой долей 40% (плотность 1,2г/мл). Определите массовые доли эфиров в смеси, если известно, что гидроксид натрия, оставшийся после гидролиза эфиров, может поглотить максимально 8,96л оксида углерода (IV). Эти задачи можно решать и другими способами, но этот способ решения задач по химии способствует формирует умение составлять и применять алгоритмы последовательности действий при решении, дисциплинирует и направляет деятельность на правильное использование физических величин и корректное проведение математических расчётов. Задача Решение задачи начинаем с построения системы координат. Конечно, удобнее использовать специальную миллиметровую бумагу, но и обычный тетрадный лист в клетку позволяет получить ответ Строя перпендикуляры из этих точек, находим точку их пересечения. пересечения с отрезком, а из точки пересечения опускаем перпендикуляр на ось х. Это ответ задачи. Задача 2. К 150 г 20%-ного раствора соли добавили 30 г соли. Определите массовую долю соли в полученном растворе. Начало решения аналогично решению задачи 1: для исходного раствора находим
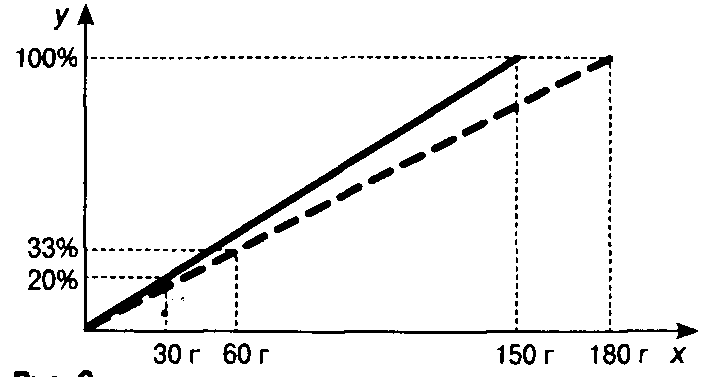
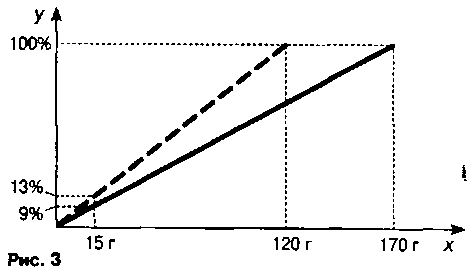
(масса добавленной соли) и получаем массу соли во втором растворе. Восстанавливаем из неё перпендикуляр до пересечения с пунктирным отрезком, а из точки пересечения — перпендикуляр на ось у. Значение^ равно массовой доле соли во втором растворе. Задача 3. Из 170 г 9%-ного раствора выпарили 50 г растворителя. Построив отрезок, соответствующий начальному раствору, находим массу растворённого
Строим отрезок для начального раствора и находим для него на оси х точку,
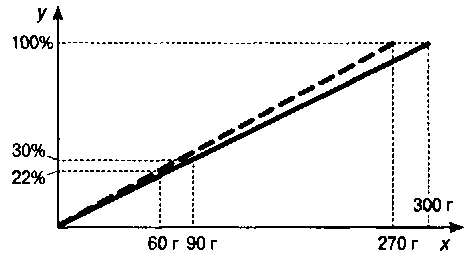
Задача Строим отрезок, соответствующий первому раствору, и находим массу растворённого в нём вещества 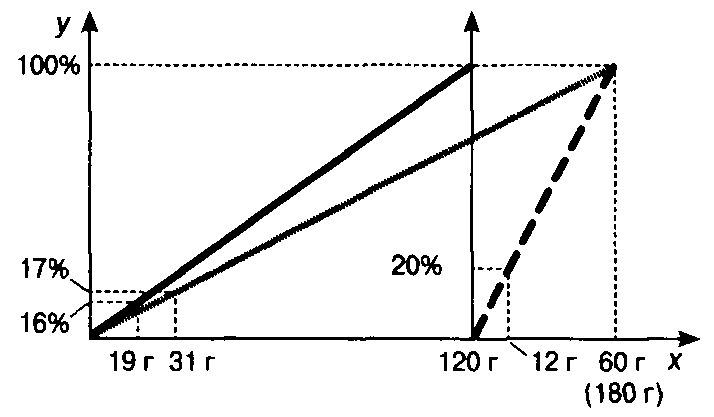 имеются два отрезка, соответствующие массам исходных растворов. Так как начало второго отрезка совпадает с концом первого, то их общая длина соответствует массе третьего раствора. Соединив точку пересечения перпендикуляров, проходящих через точки 100% и 180 г (на графике она уже получена Кроме этого, на оси х отложены два отрезка, соответствующие массам растворённых в исходных растворах О т в ет т: 17%. Конечно, данный способ решения не может рассматриваться как замена алгебраического эффективность образовательного процесса. 2. Урок – практикум «Графический метод решения химических задач»
Математика:
Ход урока Учитель химии Сегодня на уроке мы рассмотрим решения химических задач графическим методом, для Задача 1. Проанализируем условие задачи. Указаны три вещества, участвующих в химическом Вспомним, что при взаимодействии соли с кислотой получается новая соль Na²SO4 и сернистая Эта кислота по прочности какая? — 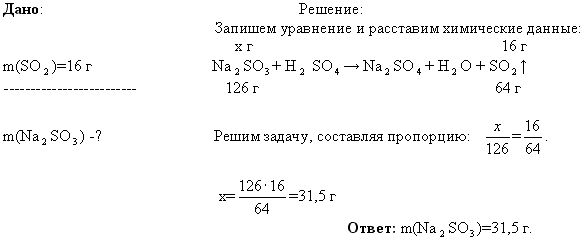 Учитель математики В ходе решения задачи данным способом выполнили следующие последовательные действия:
Учитель химии. Второй способ — это использование величины "количества вещества” и её единицы "моль”. Массу SO² переводим в количество вещества, используя формулу v =.
По уравнению реакции 1 моль Na²SO³ образует 1 моль SO², значит для получения0,25 моль SO² потребуется 0,25 моль Na²SO³, тогда m(Na²SO³)= Учитель математики Математической основой рассмотренных способов решения задач по уравнению реакции является Зависимость одной переменной от другой называют функциональной зависимостью или функцией, В данной задаче зависимость переменной m(Na²SO³) от переменной m(SO²) является функцией, т.к. каждому значению m(SO²) соответствует единственное значение m(Na²SO³). Зависимость между пропорциональными переменными выражается формулой y=kx молярной массы SO², т.е. k=126:64=1,97. Для построения графика прямой пропорциональности составляем таблицу значений Любая прямая определяется двумя своими точками. В качестве одной из таких точек целесообразно брать начало координат, а вторая точки определяется по соответствующим величинам, найденным по
Изобразим зависимость m(Na²SO³ ) от m(SO графически. Учитель химии По уравнению реакции:m(SO²)= 1 моль·64 г/моль=64 гm(Na²SO³)=1 моль·126 г/моль=126 г 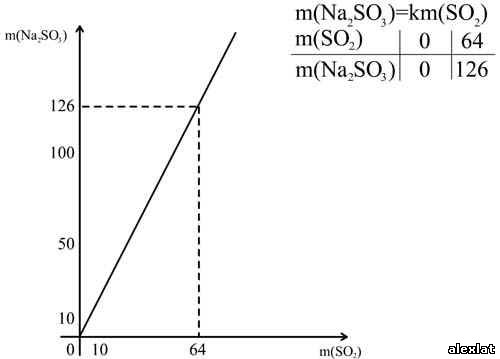 Учитель математики Для решения задачи (см. рис.) на оси абсцисс отмечаем точку, соответствующую числу 16, проводим величину массы сульфита натрия, равную 31,5 г. Для нахождения более точных значений графики рисуют или в более крупном масштабе, или 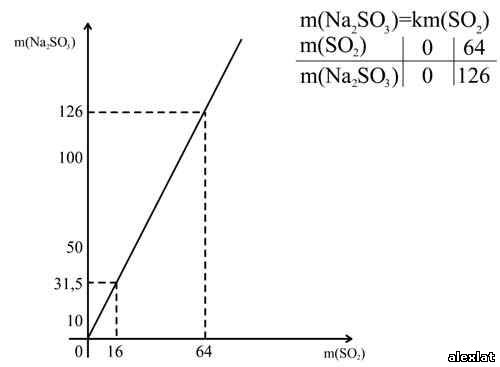 Учитель химии Подобные графические способы химических расчетов широко используются на предприятиях При решении задач на уроках химии графики практически не применяются Графический способ решения задач оказывается более рациональным при решении Задача Вычислите массу каждого из металлов, содержащихся в смеси. Проанализируем условие задачи.  Учитель математики Решим данное уравнение умножив все его части на произведение 56·65: 65·22,4x + 56·22,4· (2,33-x) = 0,896·56·65 1456x + 2922,752 - 1254,4x = 3261,44 201,6x = 338,688 x = 1,68 г (Fe) m(Zn) = 2,33 – 1,68 = 0,65 г Ответ: m(Zn) = 0,65 г. Для построения функциональной прямой нужно подсчитать объем водорода (H² ) Учитель химии Для расчета целесообразно использовать формулу: 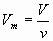 ; ;Отсюда 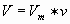 ; ;Так Определяем объем водорода, вытесненный цинком:
Определяем объем водорода, вытесненный железом:
Учитель математики Строим график прямой пропорциональной зависимости согласно таблице.
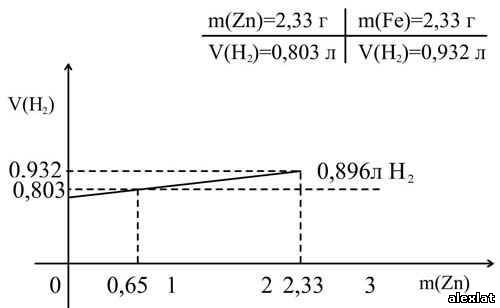
По оси абсцисс в начале координат точка 0 соответствует нулевому значению Проведем горизонтальную прямую соответствующую значению выделенного
Ответ: Учитель химии Графический способ удобен и доступен для решения задач на вывод формул веществ. Отношение индексов элементов в формуле можно найти графически. Зная, что массовая доля элемента в веществе определяется по формуле
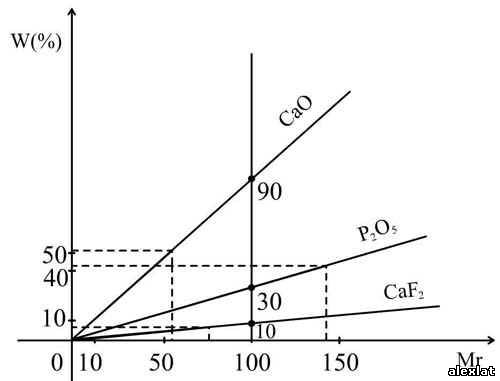
. Отношение массовой доли элемента к его относительной атомной массе представляет собой прямую. Задача
Формула минерала - ? В одной системе координат построим три графика, выражающие соотношение между величинами относительных молекулярных масс и массовыми долями тех веществ, входящих в состав минерала.; 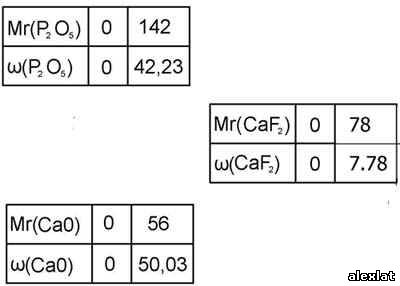 Пересечем все три функциональные прямые произвольной прямой линией, параллельной оси ординат.
Отношение точек пересечений этой прямой с функциональными прямыми:10:30:90 ( Учитель химии Ответ: формула минерала Итоги урока: Учитель химии Мы сегодня рассмотрели решения различных задач графическим методом. Учитель математики Для этого применили знания по построению графиков линейной функции к решению Учитель химии На этом уроке мы увидели, что химические задачи можно решить различными способами. Учитель математики Ваша задача – выбрать рациональный способ решения предложенной задачи. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Просмотров: 4440 | | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Всего комментариев: 0 | |
| Химия [30] |
| Золото [4] |
| Химические элементы в организме человека. [6] |
| Менделеев Дмитрий [7] |
| Органическая химия [7] |
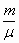
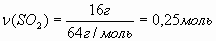
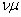 =0,25·126=31,5 г
=0,25·126=31,5 г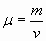 ,
, 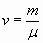 .
. 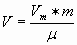 —
— 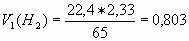 л.
л.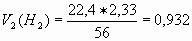 л.
л.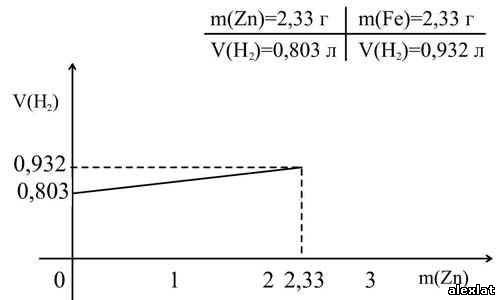
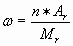 —линейная зависимость, можно найти значение
—линейная зависимость, можно найти значение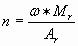
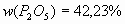
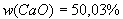
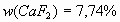
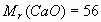 ;
; 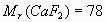 .
.
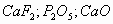 )
) 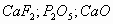 ).
).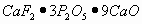 или
или