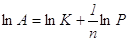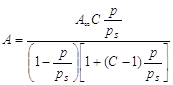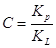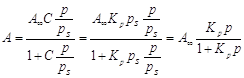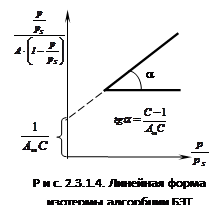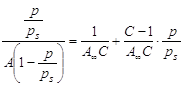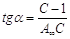| Главная » Статьи » Химия » Химия |
Адсорбционные равновесияАдсорбционное равновесие в системе "газ – жидкость". Закон Генри. Мономолекулярная адсорбция в системах "газ – жидкость", "жидкость – жидкость", "газ – твердое". Изотерма адсорбции Ленгмюра. Уравнение Фрейндлиха. Теория полимолекулярной адсорбции БЭТ. Уравнение БЭТ Предположим, что имеются компоненты-неэлектролиты. Будем считать, что адсорбат образует на поверхности адсорбента мономолекулярный слой. Мономолекулярная адсорбция с точки зрения термодинамики процесса выражается химическим потенциалом в адсорбционном слое и объемной фазе: ; ;
где При равновесии
потенциалы равны: Преобразуем:
Выражение А=а×Кг – закон Генри, т.е. при разбавлении системы коэффициент распределения стремится к постоянному значению, равному константе Генри. Если концентрация в сорбционном слое стремится к нулю, то а » с; а = ×с; à 1. Поэтому на практике закон Генри используют в следующем виде: а=Кгсi. Если одна из фаз – газ, то имеем следующий вид: a = КгРi, Кг = Кг/RT.
Эти уравнения представляют собой уравнения изотермы адсорбции при малых концентрациях. В соответствии с этими уравнениями можно по другому сформулировать закон Генри: величина адсорбции при малых давлениях газа (малых концентрациях вещества в растворе) прямо пропорциональна давлению (концентрации). Эти зависимости показаны на рисунке 2.3.1.1. При адсорбции на твердых телах область действия закона мала из-за неоднородности поверхности, но даже на однородной поверхности при увеличении концентрации обнаруживается отклонение от закона. При малых концентрациях распределенного вещества отклонения обусловлены в основном соотношением между взаимодействием молекул друг с другом и с поверхностью адсорбента. Если когезионные взаимодействия адсорбата больше, то отклонение от закона отрицательно и <1, и коэффициент распределения увеличивается (кривая 1 на рис. 2.3.1.1). Если сильнее взаимодействие "адсорбат – адсорбент", то отклонение положительно и D уменьшается (кривая 2 на рис. 2.3.1.1). При дальнейшем увеличении концентрации происходит уменьшение свободной поверхности, снижается реакционная способность и кривые загибаются к оси абсцисс. Константу Генри получают экстраполяцией коэффициента распределения на нулевую концентрацию. В соответствии с правилом фаз Гиббса в гетерогенных системах равновесные параметры зависят от дисперсности или удельной поверхности. Для адсорбционных систем эта зависимость выражается в уменьшенных концентрациях вещества в объемной фазе с увеличением удельной поверхности адсорбента. Если в такой системе содержание распределяемого вещества постоянно, то АmSуд + сV = const, где m - масса адсорбента; Sуд- удельная поверхность адсорбента; V - объем фазы, из которой извлекается вещество; const – постоянное количество вещества в системе.
D - коэффициент распределения;
Из соотношения следует, что с увеличением удельной поверхности при постоянной концентрации адсорбата концентрация уменьшается и тем сильнее, чем больше константа Генри и меньше объем фазы. Теория Ленгмюра позволяет учесть наиболее сильные отклонения от закона Генри, что связано с ограничением адсорбционного объема или поверхности адсорбента. Ограниченность этого параметра приводит к адсорбционному насыщению поверхности адсорбента по мере увеличения концентрации распределяемого вещества. Это положение уточняется следующими утверждениями. 1. Адсорбция локализована на отдельных адсорбционных центрах, каждый из которых взаимодействует только с одной молекулой адсорбента - образуется мономолекулярный слой. 2. Адсорбционные центры энергетически эквивалентны - поверхность адсорбента эквипотенциальна. 3. Адсорбированные молекулы не взаимодействуют друг с другом. Ленгмюр предположил, что при адсорбции происходит квазихимическая реакция между распределяемым компонентом и адсорбционными центрами поверхности: , где А - адсорбционые центры поверхности; В - распределенное вещество; АВ - образующийся комплекс на поверхности. Константа равновесия
процесса: где сав = А - величина адсорбции; са = А0 = А¥ - А, где А¥ - емкость адсорбционного монослоя или число адсорбционных центров, приходящихся на единицу поверхности или единицу массы адсорбента; А0 - число оставшихся свободных адсорбционных центров, приходящихся на единицу площади или единицу массы адсорбента; св – концентрация распределенного вещества. Подставляя величину концентрации в уравнение константы, получим выражения
А = А¥Кс
– АКс,
Эти выражения – уравнения изотермы адсорбции Ленгмюра. К и Кр в уравнении характеризуют энергию взаимодействия адсорбента с адсорбатом. Адсорбционное уравнение часто представляют относительно степени заполнения поверхности, т.е. как отношение А/А¥:
Экспериментальные результаты по определению изотермы адсорбции обычно обрабатывают с помощью уравнения, записанного в линейной форме;
Такая линейная зависимость позволяет графически определить А¥ и К. Зная А¥, можно определить удельную поверхность адсорбента (поверхность единицы массы адсорбента):
где А¥ - предельная адсорбция, выражаемая числом молей адсорбата на единицу массы адсорбента; NA – число Авогадро; w0 – площадь, занимаемая одной молекулой адсорбата. 1. Если сà 0, тогда уравнение примет вид: А=А¥Кс;
т.е. при сà 0 уравнение Ленгмюра переходит в уравнение Генри. 2. Если сà¥, тогда А = А¥ , А/А¥ = 1. Это случай предельной адсорбции. 3. Пусть адсорбция идет из смеси компонентов, в этом случае уравнение Ленгмюра записывается следующим образом:
Все рассмотренные выше уравнения справедливы для мономолекулярной адсорбции на адсорбенте с энергетически эквивалентными адсорбционными центрами. Однако реальные поверхности этим свойством не обладают. Приближенной к реальности является возможность распределения адсорбционных центров по энергии. Приняв линейное распределение, Темкин использовал формулу уравнения Ленгмюра и получил уравнение для средних степеней заполнения адсорбента.
где - константа, характеризующая линейное распределение; К0 - константа уравнения Ленгмюра, отвечающая максимальной теплоте адсорбции. Из уравнения следует, что увеличение парциального давления (из-за увеличения концентрации) одного компонента подавляет адсорбцию другого и тем сильнее, чем больше его адсорбционная константа равновесия. Уравнение часто называют логарифмической изотермой адсорбции. Если принять экспоненциальное распределение центров по поверхности, то в области средних заполнений получается ранее найденное эмпирическим путем уравнение Фрейндлиха:
Прологарифмировав,
получим где K, n – постоянные. Использование уравнения Фрейндлиха в логарифмической форме позволяет определить константу уравнения. Уравнение Ленгмюра можно использовать только при адсорбции в мономолекулярном слое. Это условие выполняется при хемосорбции, физической адсорбции газов при меньшем давлении и температуре выше критической.
В результате этих представлений была выведена следующая формула:
где KL = aж/ап – константа конденсации пара; аж - активность вещества в жидкости; ап - активность вещества в состоянии насыщенного пара; ап = Рs. Физический смысл С: характеризует разность энергии Гиббса в процессах чистой адсорбции и конденсации. Это уравнение получило название БЭТ (Бранауэр-Эммет- Теллер). При р/рs<<1, уравнение БЭТ превращается в уравнение Легмюра, которое при дальнейшем уменьшении давления (Рà 0) переходит в закон Генри:
При обработке экспериментальных данных уравнение БЭТ используют в линейной форме (рис. 2.3.1.4):
таким образом графически находят обе константы уравнения А¥ и С. | |
| Просмотров: 6097 | |
| Всего комментариев: 0 | |
| Химия [30] |
| Золото [4] |
| Химические элементы в организме человека. [6] |
| Менделеев Дмитрий [7] |
| Органическая химия [7] |
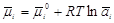
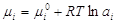
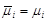
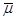
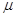
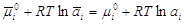
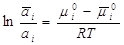
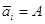
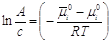
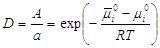
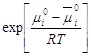
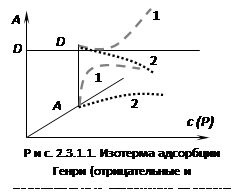
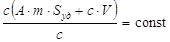
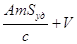
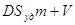
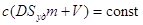 ;
;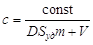 .
.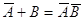
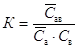
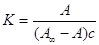
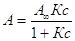
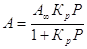
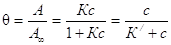
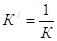
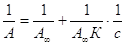
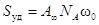
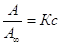
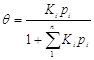
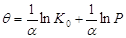
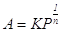 .
.